
Подготовьте компьютерную презентацию (см. § 5) по теме «Роль М. В. Ломоносова и Дж. Дальтона в создании атомно−молекулярного учения».

Роль М. В. Ломоносова и Дж. Дальтона в создании атомно−молекулярного учения
Слайд 1
Главные труды Ломоносова, в которых изложена его корпускулярная теория, это: “Элементы математической химии (1741), “276 заметок по физике и корпускулярной философии” (1741 −1743), “Опыт теории о нечувствительных частицах тел и вообще о причинах частных качеств” (1743−1744), “Физические размышления о причинах теплоты и холода” (1744), “Опыт теории упругости воздуха” (1748).

Слайд 2
М. В. Ломоносов одним из первых отказался от наивных представлений о замысловатой форме атомов. Наделив атомы массой, шарообразной формой, шероховатой поверхностью и способностью к движению, учёный объяснил процессы растворения, испарения, теплопередачи, а также высказал ряд важных положений, которые спустя 130 лет легли в основу кинетической теории газов. Путем умозрительных рассуждений М. В. Ломоносов пришёл к выводу, что все тела в природе состоят из мельчайших материальных протяженных частиц – элементов (атомов) и корпускул (молекул).
Слайд 3
Экспериментальное подтверждение атомной гипотезы нашёл английский химик Джон Дальтон. Он представил ряд докладов под общим названием «Опыты», посвященных определению состава газовых смесей, давления пара различных веществ при разных температурах в вакууме и на воздухе, испарению жидкостей, термическому расширению газов. В 1808 году Дальтон изложил свою атомистическую гипотезу в труде «Новая система химической философии».

Слайд 4
Учитывая достижения современной науки, основные положения атомно−молекулярного учения можно сформулировать так:
1) Существуют вещества с молекулярным и немолекулярным строением.
2) Между молекулами имеются промежутки, размеры которых зависят от агрегатного состояния вещества и температуры. Наибольшие расстояния имеются между молекулами газов. Этим объясняется их лёгкая сжимаемость. Труднее сжимаются жидкости, где промежутки между молекулами значительно меньше. В твёрдых веществах промежутки между молекулами ещё меньше, поэтому они почти не сжимаются.
3) Молекулы находятся в непрерывном движении. Скорость движения молекул зависит от температуры. С повышением температуры скорость движения молекул возрастает.
4) Между молекулами существуют силы взаимного притяжения и отталкивания. В наибольшей степени эти силы выражены в твёрдых веществах, в наименьшей степени — в газах.
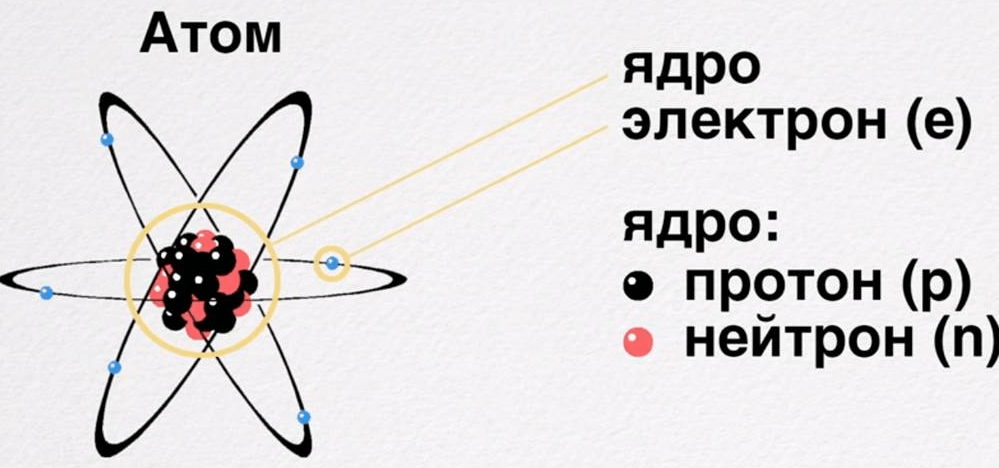
5) Молекулы состоят из атомов, которые, как и молекулы, находятся в непрерывном движении.
6) Атомы одного вида отличаются от атомов другого вида массой и свойствами.
7) При физических явлениях молекулы сохраняются, при химических явлениях они, как правило, разрушаются.
8) У веществ с молекулярным строением в твёрдом состоянии в узлах кристаллических решёток находятся молекулы. Связи между молекулами, расположенными в узлах кристаллической решётки, слабые и при нагревании разрываются. Поэтому вещества с молекулярным строением, как правило, имеют низкие температуры плавления.
9) У веществ с немолекулярным строением в узлах кристаллических решёток находятся атомы или ионы. Между этими частицами существуют прочные химические связи, для разрушения которых требуется затратить много энергии. Поэтому вещества с немолекулярным строением имеют высокие температуры плавления.
Пожалуйста, оцените решение