
Получение и свойства кислорода
В лаборатории кислород получают разложением перманганата калия. Выполняя эту работу, вы научитесь получать кислород, а также изучите его физические и химические свойства.
Реактив: перманганат калия.
Оборудование и материалы: пробирка, пробка с газоотводной трубкой, склянка для сбора кислорода, лучинка, спиртовка, спички, лабораторный штатив, воронка, вата, кусочек картона.
1) Сборка прибора
В сухую пробирку поместите перманганат калия. Какой цвет имеет это вещество? Положите в верхнюю часть пробирки кусок ваты − она будет задерживать мельчайшие частички перманганата, уносимые током выделяющегося кислорода. Плотно закройте пробирку пробкой с газоотводной трубкой и закрепите пробирку в лапке штатива практически горизонтально так, чтобы дно было немного выше, чем отверстие, а газоотводная трубка опускалась почти до дна склянки для сбора кислорода (рис. 127).
Отверстие склянки закройте кусочком картона с вырезанным в нем отверстием для газоотводной трубки.
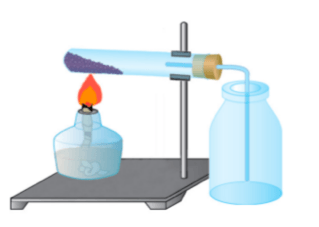
Рис. 127. Прибор для получения кислорода
2) Получение кислорода
Покажите собранный вами прибор учителю. Зажгите спиртовку. Сначала прогрейте всю пробирку, а затем нагревайте ту её часть, где находится перманганат. Что наблюдаете? По мере протекания реакции передвигайте спиртовку вдоль пробирки до тех пор, пока не разложится весь находящийся в ней перманганат калия.
3) Исследование свойств кислорода
Познакомьтесь со свойствами собранного газа. Имеет ли он цвет и запах? Что легче – воздух или кислород? Внесите в сосуд с кислородом тлеющую лучинку. Что наблюдаете? Нарисуйте прибор, составьте уравнение реакции разложения перманганата калия, запишите наблюдения. Как называется способ собирания газа, который вы использовали? Можно ли кислород собирать над водой? Напишите уравнение реакции горения угля в кислороде. Порошок, образовавшийся при разложении перманганата, необходимо высыпать в склянку для сухих отходов.

Получение и свойства кислорода
1) В сухую пробирку поместили перманганат калия. Кристаллы перманганата калия имеют темно−фиолетовый цвет. Положили в верхнюю часть пробирки кусок ваты − она будет задерживать мельчайшие частички перманганата, уносимые током выделяющегося кислорода. Плотно закрыли пробирку пробкой с газоотводной трубкой и закрепили пробирку в лапке штатива практически горизонтально так, чтобы дно было немного выше, чем отверстие, а газоотводная трубка опускалась почти до дна склянки для сбора кислорода.
Отверстие склянки закрыли кусочком картона с вырезанным в нем отверстием для газоотводной трубки.

Собранный нами прибор для получения кислорода
2) Показали собранный нами прибор учителю. Зажгли спиртовку. Сначала прогрели всю пробирку, а затем нагревали ту её часть, где находится перманганат. При нагревании перманганата калия наблюдается движение его частиц, создаётся впечатление как−будто он кипит. По мере протекания реакции передвигали спиртовку вдоль пробирки до тех пор, пока не разложится весь находящийся в ней перманганат калия.
3) Познакомились со свойствами собранного газа. Собранный газ не имеет цвета и запаха, он тяжелее воздуха, потому что кислород собрался в склянке, у которой горлышко смотрит вверх. Таким образом, газ собирали путем вытеснения воздуха. При внесении тлеющей лучинки в сосуд с кислородом, наблюдается вспыхивание лучинки.
Реакция разложения перманганата калия:
$2KMnO_{4} ⟶ K_{2}MnO_{4} + MnO_{2} + O_{2}↑$
Кислород можно собирать над водой, потому что он малорастворим в воде. Реакции горения угля в кислороде:
$C + O_{2} ⟶ CO_{2}$
Пожалуйста, оцените решение