
Получение аммиака и растворение его в воде
1) В фарфоровой ступке хорошо перемешайте приблизительно равные объёмы кристаллического хлорида аммония $NH_{4}Cl$ и порошка гидроксида кальция $Ca(OH)_{2}$ (опыт удаётся лучше, если известь слегка влажная). Приготовленную смесь насыпьте в пробирку на 1/3 её объёма. Закройте пробирку пробкой с газоотводной трубкой, конец которой опущен в другую сухую пробирку, закреплённую в штативе открытым концом вниз (рис. 22). Нагрейте смесь в пробирке.
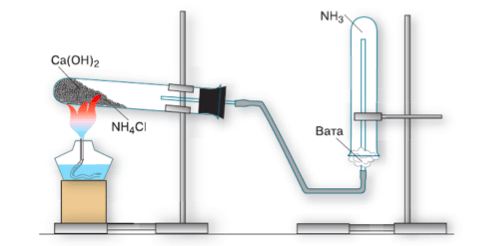
Рис. 22. Получение аммиака
2) Как только почувствуете острый запах (нюхать осторожно!), пробирку с газом, не переворачивая, закройте пробкой, погрузите её в сосуд с водой и откройте пробку.
3) После заполнения пробирки водой закройте её отверстие пробкой и выньте пробирку из воды. Половину полученного раствора перелейте в другую пробирку. В одну пробирку поместите красную лакмусовую бумагу. В другую пробирку добавьте несколько капель раствора фенолфталеина, а затем немного разбавленной соляной кислоты.
• О каких свойствах водного раствора аммиака свидетельствует его действие на индикаторы? Как это можно объяснить с позиций теории электролитической диссоциации?
• Что происходит при действии кислоты на водный раствор аммиака? Составьте уравнение соответствующей химической реакции.

Получение аммиака и растворение его в воде
1) В фарфоровой ступке хорошо перемешали приблизительно равные объёмы кристаллического хлорида аммония $NH_{4}Cl$ и порошка гидроксида кальция $Ca(OH)_{2}$. Приготовленную смесь насыпали в пробирку на 1/3 её объёма. Закрыли пробирку пробкой с газоотводной трубкой, конец которой опущен в другую сухую пробирку, закреплённую в штативе открытым концом вниз. Нагрели смесь в пробирке.
$2NH_{4}Cl + Ca(OH)_{2} = CaCl_{2} + 2H_{2}O + 2NH_{3}↑$
2) Как только почувствовали острый запах, пробирку с газом, не переворачивая, закрыли пробкой, погрузили её в сосуд с водой и открыли пробку.
$NH_{3} + H_{2}O = NH_{4}OH$
3) После заполнения пробирки водой закрыли её отверстие пробкой и вынули пробирку из воды. Половину полученного раствора перелили в другую пробирку. В одну пробирку поместили красную лакмусовую бумагу. В другую пробирку добавили несколько капель раствора фенолфталеина, а затем немного разбавленной соляной кислоты.
Лакмусовая бумага в растворе аммиака окрасилась в синий цвет. Фенолфталеин окрасил раствор в малиновый цвет.
Это говорит о том, что аммиак проявляет щелочные свойства, так как в результате диссоциации образовываются гидроксид−анионы:
$NH_{4}OH = NH_{4}^{+} + OH^{-}$
При добавлении кислоты происходит обесцвечивание фенолфталеина, так как аммиак вступает в реакцию с кислотой:
$NH_{3} + HCl = NH_{4}Cl$
Пожалуйста, оцените решение