
Напишите уравнения реакций, с помошью которых можно осуществить следующие превращения:
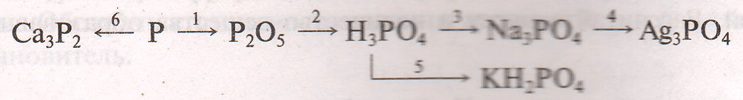
Охарактеризуйте реакцию 1 по следующим признакам:
— число и состав исходных веществ и продуктов;
— изменение степеней окисления химических элементов;
— обратимость реакции;
— участие катализатора;
— тепловой эффект.
Укажите, для каких целей в лабораториях используют реакцию 4. Составьте ионные уравнения (полное и сокрашенное) этой реакции.

1) $4P^{0} + 5O^{0}_ {2} = 2P^{+5}_{2}O^{-2}_{5}$ + Q
Число и состав исходных веществ и продуктов:
реагенты: два простых вещества;
продукты: одно сложное вещество.
Изменение степеней окисления химических элементов: происходит изменение степеней окисления.
Обратимость реакции: необратимая реакция.
Участие катализатора: нет.
Тепловой эффект: экзотермическая реакция.
2) $P_{2}O_{5} + 3H_{2}O = 2H_{3}PO_{4}$
3) $H_{3}PO_{4} + 3NaOH = Na_{3}PO_{4} + 3H_{2}O$
4) $Na_{3}PO_{4} + 3AgNO_{3} = Ag_{3}PO_{4}↓ + 3NaNO_{3}$
$3Na^{+} + PO_{4}^{3-} + 3Ag^{+} + 3NO_{3}^{-} = Ag_{3}PO_{4}↓ + 3Na^{+} + 3NO_{3}^{-}$
$PO_{4}^{3-} + 3Ag^{+} = Ag_{3}PO_{4}↓$
Реакцию используют для получения фосфата серебра.
5) $H_{3}PO_{4} + KOH = KH_{2}PO_{4} + H_{2}O$
6) $3Ca + 2P = Ca_{3}P_{2}$
Пожалуйста, оцените решение