
Используя график зависимости растворимости веществ от температуры (рис. 1), определите массу кристаллов хлоридов аммония $NH_{4}Cl$, которые образуются при охлаждении 100 г насыщенного раствора этой соли от t = 90℃ до t = 30℃.
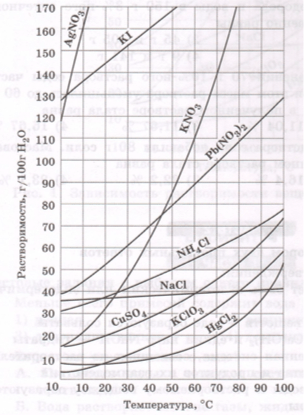
Рис. 1. Зависимость растворимости веществ от температуры

Дано:
m (р−ра) = 100 г
t = 90℃
$t_{1}$ = 30℃
S (растворимость) = 70 г / 100 г $H_{2}O$
$S_{1}$ (растворимость) = 40 г / 100 г $H_{2}O$
Найти:
m (кристаллов) − ?
Решение:
ω = $\frac{m (в-ва)}{m (р-ра)}$ * 100% = $\frac{70}{70\;+\;100}$ = 41,2%
m ($CuSO_{4}$) = m (р−ра) * ω = 100 * 0,412 = 41,2 г
$ω_{1}$ = $\frac{m (в-ва)}{m (р-ра)}$ * 100% = $\frac{40}{40\;+\;100}$ = 28,6%
$m_{1}$ ($CuSO_{4}$) = m (р−ра) * ω = 100 * 0,286 = 28,6 г
m (кристаллов) = m ($NH_{4}Cl$) − $m_{1}$ ($NH_{4}Cl$) = 41,2 − 28,6 = 12,6 г
Ответ: m (кристаллов) = 12,6 г.
Пожалуйста, оцените решение